Содержание
Что относится к тяжелым металлам
На сегодняшний день известно порядка 40 различных трактовок термина «тяжелые металлы», и совершенно невозможно выделить одну наиболее правильную. Так, каждое определение тяжелых металлов будет включать свой перечень элементов согласно с теми или иными критериями. Зачастую характеристика тяжелых металлов основывается на: атомной массе, плотности, токсичности, распространенности в природной среде, степени вовлеченности в природные и техногенные циклы. Например, основным критерием может являться минимальная относительная атомная масса, равная 50. Согласно данной особенности, под список «тяжелых металлов» попадут абсолютно все металлы, начиная с ванадия, вне зависимости от их плотности. Однако, в других определениях данного термина именно плотность является главной характеристикой, на основе которой и составляется перечень, и она должна быть более или равной 8 г/см 3 (плотность железа). Согласно данному критерию в список «тяжелых металлов» будут включены следующие элементы: свинец, ртуть, медь, кадмий, кобальт, а вот олово уже будет исключено из данного списка, так оно более легкое. Кроме того, также в основе классификации металлов могут находится и другие значения пороговой плотности (например, в 5 г/см 3 ) или атомной массы. Таким образом, к некоторым группа тяжелых металлов могут попадать элементы, которые являются хрупкими или металлоидами (например, висмут или мышьяк, соответственно). В связи с этим, термин «тяжелые металлы» рассматривается с медицинской и природоохранной точек зрения. Это позволяет при составлении списка тяжелых металлов основываться не только на физических и химический свойствах элемента, но и на его биологической активности, токсичности, а также объеме его применения в хозяйственной деятельности.
Однако, все же в большинстве случаев, в список тяжелых металлов входит 40 элементов, имеющие относительную плотность, превышающую 6. Не смотря на то, что термин «тяжелые металлы» и «токсичные металлы» принято считать синонимами, все же количество опасных металлов существенно меньше, что не может не радовать.
В первую очередь интерес представляют элементы, имеющие самое широкое и активное использование в производстве, в результате чего происходит их накопление в окружающей среде, что и представляет опасность здоровью человечества с точки зрения их биологической активности и токсичности. Среди таковых следует выделить свинец, ртуть, кадмий, цинк, висмут, кобальт, никель, медь, олово, сурьму, ванадий, марганец, хром, молибден и мышьяк.
Свойства тяжелых металлов
Тяжелые металлы в атмосфере представляют собой органические и неорганические соединения. Они могут присутствовать как пыль, аэрозоль, или же иметь газообразную элементную форму (например, ртуть). Стоит отметить, что свинец, кадмий, медь и цинк в виде аэрозоля включают в себя, главным образом, субмикронные частицы, диаметр которых составляет примерно 0,5 – 1 мкм. А вот частицы никеля и кобальта в виде аэрозоля представляют собой крупнодисперсные частицы, имеющие диаметр, превышающий 1 мкм. Их образование, в основном, происходит во время сгорания дизельного топлива.
В водной среде тяжелые металлы могут быть представлены в виде трех основных форм: взвешенных частиц, коллоидных частиц, а также растворенных соединений. Последние представляют собой свободные ионы и растворимые комплексные соединения с органическими (гуминовые и фульвокислоты) и неорганическими (галогены, сульфаты, фосфаты, карбонаты) лигандами. Форма нахождения элемента в воде определяется гидролизом, который очень сильно влияет на нахождение указанных элементов в водной среде. Огромное количество тяжелых металлов переносится посредством поверхностных вод во взвешенном состоянии.
Содержание тяжелых металлов в почвах представлено водорастворимой, ионообменной и непрочно адсорбированной формах. Первые, главным образом, представляют собой хлориды, нитраты, сульфаты, а также органические комплексные соединения. Следует сказать, что часто отмечается связь ионов тяжелых металлов с минералами почвы, как часть кристаллической решетки.
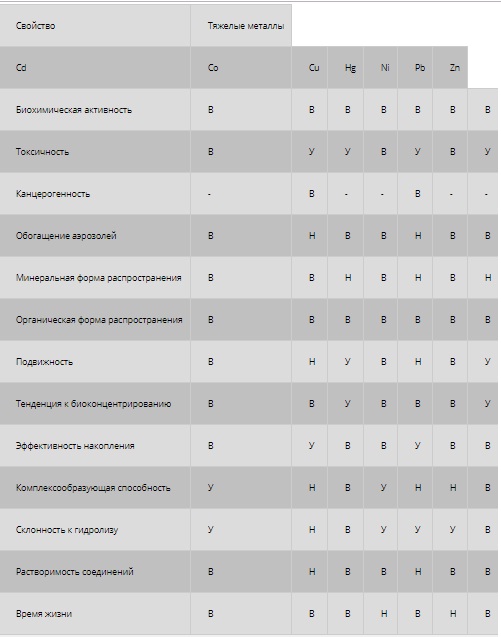
В таблице представлены биогеохимические свойства тяжелых металлов, оценка которых осуществлялась по трем главным критериям: высокая (В), умеренная (У), низкая (Н).
Стоит отметить, что к биогеохимическим свойствам тяжелых металлов относятся токсичность, канцерогенность, растворимость и многие другие, которые выражены у них по-разному. Однако, существует два основных свойства, на основе которых и определяется степень опасности того или иного тяжелого металла для живого организма в зависимости от концентрации. К данным свойствам относятся: биохимическая активность и органическая форма распространения.
Определение тяжелых металлов
На сегодняшний день есть две главные группы аналитических методов, которые позволяют определять тяжелые металлы (например, в воде или почве), а именно:
- электрохимические методы;
- спектрометрические методы.
Стоит отметить что вторая группа постепенно сдает свои позиции и уступает электрохимическим методам.

Среди спектрометрических методов следует выделить наиболее распространенный – атомно-абсорбционную спектрометрию с разной атомизацией образцов. В том случае, когда необходимо определить несколько элементов одновременно, главным методом определения выступают атомная эмиссионная спектрометрия с индукционно связанной плазмой, а также масс-спектрометрия с индукционно связанной плазмой.
Для того, чтобы определить тяжелые металлы электрохимическими способами пробу переводят в водный раствор. К электрохимическим методам относятся: полярографический (вольтамперометрический), потенциометрический, кулонометрический, кондуктометрический и многие другие. Стоит отметить, что бывают ситуации, когда невозможно определить тяжелые металлы с помощью лишь только одного метода, тогда используются сразу несколько методов с дальнейшим титрованием. Данные методы основываются на анализе вольт-амперных характеристик, потенциалов ион-селективных электродов, интегрального заряда, который служит для того, чтобы искомый метал выпал в осадок на электроде электрохимической ячейке, электропроводности раствора и т.д. Указанные способы позволяют определять тяжелые металлы до 10 -9 моль/л.
Группа спектральных анализов является включает в себя множество различных методов, с помощью которых осуществляется определение тяжелых металлов. Прежде всего, она включает в свой перечень атомный эмиссионный анализ, атомный абсорбционный анализ, спектрофотометрию, масс-спектрометрию, спектрометрию с индуктивно связанной плазмой, рентгеноспектральный анализ.
В отдельных случаях, когда концентрация тяжелых металлов находится в достаточно небольшой концентрации, то они определяются, зачастую, несколькими методами спектрометрии.
Иногда, для определения тяжелых металлов, следует прибегнуть к комплексным методам, которые сочетают в себе как спектральные, как и электрохимические способы. Одним из таких методов является спектрополяриметральный анализ.
Самый тяжелый металл
Определить и назвать один единственный самый тяжелый металл невозможно, так как критерии определения «тяжести» металла могут быть совершенно разными. Об этом шла речь в начале данной статьи. Таким образом, одним из самых тяжелых металлов является свинец, которому не уступают цинк, олово, железо, и медь, однако он не может носить титул самого тяжелого металла. Например, свинец существенно уступает жидкому металлу – ртути. Так, если поместить в ртуть кусочек свинца, то он не утонет, а будет уверенно держаться на ее поверхности. Бутылка с ртутью объемом в 1 литр будет весить 14 кг. Но, не смотря на это, и ртуть не является самым тяжелым металлом, так как золото и платина тяжелее ртути в полтора раза.
Опережают золото и платину редкие металлы – иридий и осмий, которые в два раза тяжелее железа. Итак, самые тяжелые металлы, согласно их удельному весу:
- цинк – 7,1;
- олово – 7,3;
- железо – 7,8;
- медь – 8,9;
- свинец – 11,3;
- ртуть – 13,6;
- золото – 19,3;
- платина – 21,5;
- иридий – 22,4;
- осмий – 22,5
Если же взять за основную характеристику тяжелых металлов плотность, то список будет отличаться, и в него войдут следующие элементы:
- тантал – 16,67 г/см 3 ;
- уран – 19,05 г/см 3 ;
- вольфрам – 19,29 г/см 3 ;
- золото – 19,29 г/см 3 ;
- плутоний – 19,80 г/см 3 ;
- нептуний – 20,47 г/см 3 ;
- рений – 21,01 г/см 3 ;
- платина – 21,40 г/см 3 ;
- осмий – 22,61 г/см 3 ;
- иридий – 22,65 г/см 3 ;
Однако, существует перечень металлов, которых общепринято считать тяжелыми. Основные тяжелые металлы:
Особенности тяжелых металлов заключаются в том, что все они обладают высокой токсичностью и в некоторых случаях несут угрозу здоровью и жизни живых организмов. Кроме этого, они обладают способностью к биоаккумуляции и биомагнификации.
Применение тяжелых металлов
В далекие времена появившиеся первые металлы в жизни человека существенно облегчили его существование на Земле. Ведь металл является более прочным материалом, чем камень или дерево. Из металла получались более продуктивные орудия труда, более разрушительное оружие, а также более надежная защита. Кроме этого, из металла люди также научились изготавливать украшения, посуду, различные ритуальные предметы, а также предметы повседневного обихода. На сегодняшний день человечеству известно порядка 70 металлов, часть из которых, согласно разным определениям и критериям отбора, являются тяжелыми. Благодаря своим уникальным свойствам и особенностям, тяжелые металлы нашли свое применение во многих сферах человеческой деятельности, в частности, в машиностроении, судостроении, авиастроении, медицине, производстве техники и электроники, строительстве, в производстве посуды, украшений, а также вещей повседневного обихода.

Например, свинец используется для покрытия различной аппаратуры с целью ее защиты от коррозии. Также его используют в качестве оболочки кабелей, которые прокладываются под землей, в воде или любой другой влажной среде. Для зажигания двигателей внутреннего сгорания все так же используются свинцовые аккумуляторы, не смотря на то, что уже в природе давно существуют никелевые аккумуляторы, однако, стоимость последних значительно выше.
Ртуть также нашла свое широкое применение в электротехнике, электронике, приборостроении, металлургии, химии (изготовление термометров, барометров, реле, лампы дневного света, кварцевые ртутные лампы) и т.д.
Медь благодаря своему низкому удельному сопротивлению и высокой теплопроводности, достаточно широко используется в электротехнике – она является основным материалом, из которого производят силовые и другие кабели, провода, другие проводники. Из меди изготавливают различные теплообменники – радиаторы охлаждения, кондиционирования, отопления, компьютерные кулеры, тепловые трубки и многое другое.
Данные элементы добываются из руды тяжелых металлов – изначально извлекается руда, после чего осуществляется ее обогащение и затем при помощи химического или электролитического восстановления уже получается сам металл.
Тяжелые металлы
Что такое тяжелые металлы
Особое значение приобрело загрязнение биосферы группой полютантов, получивших общее название “тяжелые металлы”. К ним относится более 40 химических элементов периодической системы Д. И. Менделеева.
Тяжелыми металлами являются хром, марганец, железо, кобальт, никель, медь, цинк, галлий, германий, молибден, кадмий, олово, сурьма, теллур, вольфрам, ртуть, таллий, свинец, висмут. Употребляемый иногда термин “токсические элементы” здесь неудачен, так как любые элементы и их соединения могут стать токсичными для живых организмов при определенной концентрации и условиях окружающей среды.
Главным природным источником тяжелых металлов являются породы (магматические и осадочные) и породообразующие минералы. Многие минералы в виде высокодисперсных частиц включаются в качестве акцессорных (микропримесей) в массу горных пород. Примером таких минералов являются минералы титана (брусит, ильменит, анатаз), хрома (FeCr2O4). Многие элементы поступают в атмосферу с космической и метеоритной пылью, с вулканическими газами, горячими источниками, газовыми струями.
Поступление тяжелых металлов в биосферу вследствие техногенного рассеивания осуществляется разнообразными путями. Важнейшим из них является выброс при высокотемпературных процессах в черной и цветной металлургии, при обжиге цементного сырья, сжигании минерального топлива. Кроме того, источником загрязнения биоценозов могут служить орошение водами с повышенным содержанием тяжелых металлов, внесение осадков бытовых сточных вод в почвы в качестве удобрения. Вторичное загрязнение происходит также вследствие выноса тяжелых металлов из отвалов рудников или металлургических предприятий водными или воздушными потоками, поступления больших количеств тяжелых металлов при постоянном внесении высоких доз органических, минеральных удобрений и пестицидов, содержащих тяжелые металлы.
Часть техногенных выбросов тяжелых металлов, поступающих в атмосферу в виде аэрозолей, переносится на значительное расстояние и вызывает глобальное загрязнение. Другая часть с гидрохимическим стоком попадает в бессточные водоемы, где накапливается в водах и донных отложениях и может стать источником вторичного загрязнения. Соединения тяжелых металлов сравнительно быстро распространяются по объемам водного объекта. Частично они выпадают в осадок в виде карбонатов, сульфатов, частично адсорируются на минеральных и органических осадках. В результате содержание тяжелых металлов в отложениях постоянно растет, и когда абсорбционная способность осадков исчерпывается и тяжелые металлы поступают в воду, возникает особо напряженная ситуация. Этому способствует повышение кислотности воды, сильное зарастание водоемов, интенсификация выделения СО2 в результате деятельности микроорганизмов. Значительное загрязнение тяжелыми металлами, особенно свинцом, а также цинком и кадмием обнаружено вблизи автострад. Ширина придорожных аномалий свинца в почве достигает 100 м и более.
Тяжелые металлы, поступающие на поверхность почвы, накапливаются в почвенной толще, особенно в верхних гумусовых горизонтах, и медленно удаляются при выщелачивании, потреблении растениями, эрозии. Первый период полуудаления (т.е. удаления половины от начальной концентрации) тяжелых металлов значительно варьируется у различных элементов и занимает весьма продолжительный период времени: для цинка – от 70 до 510 лет; кадмия от 13 до 11О лет, меди -от 310 до 1500 лет, свинца – от 770 до 5900 лет.
Тяжелые металлы способны образовывать сложные комплексные соединения с органическими веществами почвы, поэтому в почвах с высоким содержанием гумуса они менее доступны для полощения. Избыток влаги в почве способствует переходу тяжелых металлов в низшие степени окисления и в растворимые формы. Анаэробные условия повышают доступность тяжелых металлов растениям. Поэтому дренажные системы, регулирующие водный режим, способствуют преобладанию окисленных форм тяжелых металлов и тем самым снижению их миграционных характеристик. Растения могут поглотать из почвы микроэлементы, в том числе тяжелые металлы, аккумулируя их в тканях или на поверхности листьев, являясь, таким образом, промежуточным звеном в цепи “почва – растение – животное – человек”.
Различные растения сосредоточивают в себе разное число микроэлементов: в большинстве случаев – избирательно. Так, медь усваивают растения семейства гвоздичных, кобальт – перцы. Высокий коэффициент биологического поглощения цинка характерен для березы карликовой и лишайников, никеля и меди – для вероники и лишайников. Тяжелые металлы являются протоплазматическими ядами, токсичность которых возрастает по мере увеличения атомной массы. Их токсичность проявляется по-разному. Многие металлы при токсичных уровнях концентраций ингибируют деятельность ферментов (медь, ртуть). Некоторые из них образуют хелатоподобные комплексы с обычными метаболитами, нарушая нормальный обмен веществ (железо). Такие металлы, как кадмий, медь, железо, взаимодействуют с клеточными мембранами, изменяя их проницаемость.
Особый интерес представляет изучение животных, являющихся чувствительным индикатором начальных стадий загрязнения тяжелыми металлами. Они аккумулируют элементы в доступных биологически активных формах и отражают фактический уровень загрязнения экосистем. Почвенные животные, особенно сапрофитные группы, благодаря тесной связи с почвенными условиями и ограниченной территорией обитания могут быть хорошими индикаторами химического загрязнения биосферы. Среди животных такими индикаторами могут быть европейский крот, бурый медведь, лось, рыжая полевка. Располагая сведениями о содержании тяжелых металлов у млекопитающих, можно прогнозировать их влияние на организм человека.
Что относится к тяжелым металлам
Кадмий является относительно редким и рассеянным элементом, в природе концентрируется в минералах цинка. Поступает в природные воды в результате смыва почв, выветривания полиметаллических и медных руд, и со сточными водами рудообогатительных, металлургических и химических производств. Кадмий в норме присутствует в организме человека в микроскопических количествах. При накоплении организмом соединений кадмия поражается нервная система, нарушается фосфорно-кальциевый обмен. Хроническое отравление приводит к анемии и разрушению костей.
Тяжелые металлы — Heavy metals

Тяжелые металлы обычно определяются как металлы с относительно высоким плотности, атомные веса, или же атомные номера. Используемые критерии и металлоиды включены, различаются в зависимости от автора и контекста. [2] В металлургиянапример, тяжелый металл может быть определен на основе плотности, тогда как в физике критерием различия может быть атомный номер, в то время как химик, вероятно, будет больше интересоваться химическое поведение. Были опубликованы более конкретные определения, но ни одно из них не получило широкого признания. Определения, рассматриваемые в этой статье, охватывают до 96 из 118 известных химические элементы; Только Меркурий, вести и висмут встретить их всех. Несмотря на это отсутствие согласия, термин (множественное или единственное число) широко используется в науке. Плотность более 5 г / см 3 иногда цитируется как часто используемый критерий и используется в основной части этой статьи.
Самые ранние известные металлы — обычные металлы, такие как утюг, медь, и банка, и драгоценные металлы, такие как серебро, золото, и платина- тяжелые металлы. С 1809 г. легкие металлы, Такие как магний, алюминий, и титан, были обнаружены, а также менее известные тяжелые металлы, включая галлий, таллий, и гафний.
Некоторые тяжелые металлы являются незаменимыми питательными веществами (обычно железо, кобальт, и цинк) или относительно безвредны (например, рутений, серебро и индий), но может быть токсичным в больших количествах или в определенных формах. Другие тяжелые металлы, такие как кадмий, ртуть и свинец очень ядовиты. Возможные источники отравления тяжелыми металлами включают: добыча полезных ископаемых, хвосты, промышленные отходы, сельскохозяйственные стоки, профессиональное облучение, краски и обработанная древесина.
К физическим и химическим характеристикам тяжелых металлов следует относиться с осторожностью, поскольку соответствующие металлы не всегда определяются последовательно. Помимо того, что тяжелые металлы относительно плотны, они, как правило, менее реактивный чем более легкие металлы и имеют гораздо меньше растворимый сульфиды и гидроксиды. Хотя относительно легко отличить тяжелый металл, такой как вольфрам из более легкого металла, такого как натрий, некоторые тяжелые металлы, такие как цинк, ртуть и свинец, обладают некоторыми характеристиками более легких металлов, а более легкие металлы, такие как бериллий, скандий, и титан обладают некоторыми характеристиками более тяжелых металлов.
Тяжелые металлы относительно редки в земной коры но присутствуют во многих аспектах современной жизни. Они используются, например, в гольф-клубы, легковые автомобили, антисептики, самоочищающиеся печи, пластмассы, солнечные панели, мобильные телефоны, и ускорители частиц.
Содержание
Определения
Шесть элементов ближе к концу периоды (строки) 4-7, иногда рассматриваемые металлоиды, рассматриваются здесь как металлы: они германий (Ge), мышьяк (В качестве), селен (Se), сурьма (Сб), теллур (Te) и астатин (В). [16] [n 2] Оганессон (Og) считается неметаллом.
Не существует общепризнанного критериального определения хэви-метала. Термин может иметь разные значения в зависимости от контекста. В металлургия, например, тяжелый металл может быть определен на основе плотность, [17] тогда как в физике отличительным критерием может быть атомный номер, [18] а химика или биолога, вероятно, больше интересует химическое поведение. [10]
Критерии плотности от более 3,5 г / см 3 до более 7 г / см 3 . [3] Определения атомного веса могут варьироваться от более чем натрий (атомный вес 22,98); [3] больше 40 (без учета s- и f-блок металлов, следовательно, начиная с скандий); [4] или более 200, т.е. от Меркурий вперед. [5] Атомные номера тяжелых металлов обычно превышают 20 (кальций); [3] иногда он ограничивается 92 (уран). [6] Определения, основанные на атомном номере, критиковались за включение металлов с низкой плотностью. Например, рубидий в группа (столбец) 1 из периодическая таблица имеет атомный номер 37, но плотность всего 1,532 г / см 3 , что ниже порогового значения, используемого другими авторами. [19] Та же проблема может возникнуть с определениями на основе атомного веса. [20]
В Фармакопея США включает тест на тяжелые металлы, который включает осаждение металлических примесей по мере их окрашивания сульфиды.» [7] [n 3] В 1997 году Стивен Хоукс, профессор химии, писавший в контексте своего пятидесятилетнего опыта использования этого термина, сказал, что он применяется к «металлам с нерастворимыми сульфидами и гидроксиды, чей соли производить цветные растворы в воде и комплексы обычно окрашены ». На основе металлов, которые он видел, называемых тяжелыми металлами, он предположил, что было бы полезно определить их как (в целом) все металлы в столбцах периодической таблицы. 3 к 16 которые находятся в ряд 4 или больше, другими словами, переходные металлы и постпереходные металлы. [10] [n 4] В лантаноиды удовлетворять трехчастному описанию Хокса; статус актиниды не полностью решен. [n 5] [n 6]
В биохимия, тяжелые металлы иногда определяют — на основе Кислота Льюиса (акцептор электронных пар) поведение их ионов в водном растворе — как класса B и пограничных металлов. [41] В этой схеме ионы металлов класса А предпочитают кислород доноры; ионы класса B предпочитают азот или же сера доноры; и пограничные или амбивалентные ионы демонстрируют характеристики класса A или B, в зависимости от обстоятельств. [n 7] Металлы класса А, которые, как правило, имеют низкую электроотрицательность и формировать связи с большими ионный характер, являются щелочь и щелочноземельные земли, алюминий, то металлы 3 группы, а также лантаноиды и актиниды. [n 8] Металлы класса B, которые, как правило, имеют более высокую электроотрицательность и образуют связи со значительными ковалентный характером, в основном являются более тяжелые переходные и постпереходные металлы. Пограничные металлы в основном включают более легкие переходные и постпереходные металлы (плюс мышьяк и сурьма). Различие между металлами класса А и двумя другими категориями резкое. [45] Часто цитируемое предложение [n 9] использовать эти классификационные категории вместо более запоминающихся [11] имя тяжелый металл не получил широкого распространения. [47]
Список тяжелых металлов по плотности
Плотность более 5 г / см 3 иногда упоминается как общий определяющий фактор тяжелых металлов [48] и, в отсутствие единодушного определения, используется для заполнения этого списка и (если не указано иное) для направления оставшейся части статьи. Металлоиды, отвечающие применимым критериям, например мышьяк и сурьма, иногда считаются тяжелыми металлами, особенно в химия окружающей среды, [49] как здесь. Селен (плотность 4,8 г / см 3 ) [50] также включен в список. Он незначительно не соответствует критерию плотности и менее известен как металлоид. [16] но имеет химический состав на водной основе, в некоторых отношениях сходный с мышьяком и сурьмой. [51] Другие металлы, которые иногда классифицируются или рассматриваются как «тяжелые» металлы, например бериллий [52] (плотность 1,8 г / см 3 ), [53] алюминий [52] (2,7 г / см 3 ), [54] кальций [55] (1,55 г / см 3 ), [56] и барий [55] (3,6 г / см 3 ) [57] здесь рассматриваются как легкие металлы и, как правило, далее не рассматриваются.
-
¶ ¶ ¶ ¶ ¶ ¶ ¶
Происхождение и использование термина
Тяжесть встречающиеся в природе металлы Такие как золото, медь, и утюг мог быть замечен в предыстория и в свете их пластичность, привели к первым попыткам изготовления металлических украшений, инструментов и оружия. [64] Все металлы, открытые с тех пор до 1809 года, имели относительно высокую плотность; их тяжесть считалась исключительно отличительным критерием. [65]
С 1809 г. легкие металлы, такие как натрий, калий и стронций были изолированы. Их низкая плотность противоречит общепринятым представлениям, и было предложено называть их металлоиды (что означает «напоминающие металлы по форме или внешнему виду»). [66] Это предложение было проигнорировано; новые элементы стали называть металлами, а затем термин «металлоид» использовался для обозначения неметаллических элементов, а позднее элементов, которые было трудно описать как металлы или неметаллы. [67]
Термин «тяжелый металл» впервые был использован в 1817 году, когда немецкий химик Леопольд Гмелин разделил элементы на неметаллы, легкие металлы и тяжелые металлы. [68] Легкие металлы имели плотность 0,860–5,0 г / см3. 3 ; тяжелые металлы 5.308–22.000. [69] [n 10] Позднее этот термин стал ассоциироваться с элементами с высоким атомным весом или высоким атомным номером. [19] Иногда он используется как синонимы термина тяжелый элемент. Например, обсуждая историю ядерная химия, Маги [70] отмечает, что когда-то считалось, что актиниды представляют новую группу переходных тяжелых элементов, тогда как Сиборг и коллеги «предпочитали . тяжелый металл редкоземельный как сериал . ». астрономияОднако тяжелый элемент — это любой элемент тяжелее, чем водород и гелий. [71]
Критика
В 2002 году шотландский токсиколог Джон Даффус проанализировал определения, использованные за предыдущие 60 лет, и пришел к выводу, что они настолько разнообразны, что фактически лишают этот термин смысла. [72] Наряду с этим открытием, статус тяжелых металлов для некоторых металлов иногда ставится под сомнение на том основании, что они слишком легкие, или участвуют в биологических процессах, или редко представляют опасность для окружающей среды. Примеры включают скандий (слишком легкий); [19] [73] ванадий к цинк (биологические процессы); [74] и родий, индий, и осмий (слишком редко). [75]
Популярность
Несмотря на сомнительное значение, термин тяжелый металл регулярно появляется в научной литературе. Исследование 2010 года показало, что он все чаще используется и, похоже, стал частью языка науки. [76] Считается, что это приемлемый термин, учитывая его удобство и известность, если он сопровождается строгим определением. [41] Аналоги тяжелых металлов, легкие металлы, упоминаются Общество минералов, металлов и материалов как включая «алюминий, магний, бериллий, титан, литий, и другие химически активные металлы ». [77] Названные металлы имеют плотность от 0,534 до 4,54 г / см. 3 .
Биологическая роль
| Элемент | Миллиграммы [78] | |
|---|---|---|
| Утюг | 4000 | 4000 |
Следы некоторых тяжелых металлов, в основном в период 4, необходимы для определенных биологических процессов. Это утюг и медь (кислород и электронный транспорт); кобальт (сложные синтезы и клеточный метаболизм); цинк (гидроксилирование); [83] ванадий и марганец (регуляция ферментов или функционирующий); хром (глюкоза утилизация); никель (рост клеток); мышьяк (метаболический рост у некоторых животных и, возможно, у людей) и селен (антиоксидант функционирование и гормон производство). [84] Периоды 5 и 6 содержат меньше основных тяжелых металлов, что согласуется с общей закономерностью, согласно которой более тяжелые элементы, как правило, менее распространены, а более дефицитные элементы с меньшей вероятностью являются необходимыми с точки зрения питания. [85] В период 5, молибден требуется для катализ из редокс реакции; кадмий используется некоторыми морскими диатомеи с той же целью; и банка может потребоваться для роста у некоторых видов. [86] В период 6, вольфрам требуется некоторыми археи и бактерии для метаболические процессы. [87] Дефицит любого из этих 4-6 основных тяжелых металлов может повысить восприимчивость к отравление тяжелыми металлами [88] (наоборот, избыток также может иметь неблагоприятные биологические эффекты). В среднем 70 кг тело человека составляет около 0,01% тяжелых металлов (
7 г, что эквивалентно весу двух сушеных горохов, с железом — 4 г, цинком — 2,5 г и свинцом — 0,12 г, включая три основных компонента), 2% легких металлов (
1,4 кг, вес бутылки вина) и почти 98% неметаллов (в основном воды). [89] [n 15]
Было обнаружено, что некоторые несущественные тяжелые металлы обладают биологическим действием. Галлий, германий (металлоид), индий и большинство лантаноидов могут стимулировать метаболизм, а титан способствует росту растений [90] (хотя это не всегда считается тяжелым металлом).
Токсичность
Часто считается, что тяжелые металлы очень токсичны или вредны для окружающей среды. [91] Некоторые из них токсичны, в то время как другие токсичны, только если их принимать в избытке или встречаться в определенных формах.
Экологические тяжелые металлы
Хром, мышьяк, кадмий, ртуть и свинец обладают наибольшим потенциалом причинения вреда из-за их широкого использования. токсичность некоторых из их комбинированных или элементарных форм, а также их широкое распространение в окружающей среде. [92] Шестивалентный хром, например, очень токсичен, как и пары ртути и многие соединения ртути. [93] Эти пять элементов имеют сильное сродство с серой; в человеческом теле они обычно связываются через тиол группы (–SH), чтобы ферменты отвечает за контроль скорости метаболических реакций. Образовавшиеся связи сера-металл препятствуют правильному функционированию задействованных ферментов; здоровье человека ухудшается, иногда со смертельным исходом. [94] Хром (в его шестивалентной форме) и мышьяк являются канцерогены; кадмий вызывает дегенеративная болезнь костей; а ртуть и свинец повреждают Центральная нервная система.





Свинец является наиболее распространенным загрязнителем тяжелых металлов. [95] Уровни в водной среде индустриальных обществ, по оценкам, в два-три раза выше, чем доиндустриальные уровни. [96] В составе тетраэтилсвинец, (CH
3 CH
2 )
4 Pb , он широко использовался в бензин в течение 1930–1970-х гг. [97] Хотя к 1996 году использование этилированного бензина в Северной Америке было в значительной степени прекращено, в почвах рядом с дорогами, построенными до этого времени, сохраняется высокая концентрация свинца. [98] Более поздние исследования продемонстрировали статистически значимую корреляцию между уровнем использования этилированного бензина и насильственными преступлениями в Соединенных Штатах; с учетом отставания во времени в 22 года (для среднего возраста жестоких преступников) кривая насильственных преступлений практически повторяет кривую воздействия свинца. [99]
Другие тяжелые металлы, известные своей потенциально опасной природой, обычно как токсичные загрязнители окружающей среды, включают марганец (поражение центральной нервной системы); [100] кобальт и никель (канцерогены); [101] медь, [102] цинк [103] селен [104] и серебро [105] (эндокринный нарушение врожденные нарушенияили общие токсические эффекты для рыб, растений, птиц или других водных организмов); жесть, как оловоорганическое вещество (поражение центральной нервной системы); [106] сурьма (подозреваемый канцероген); [107] и таллий (поражение центральной нервной системы). [102] [n 16] [n 17]
Важные в питании тяжелые металлы
Тяжелые металлы, необходимые для жизни, могут быть токсичными, если их принимать в избытке; некоторые имеют особенно токсичные формы. Пятиокись ванадия (V2О5) является канцерогенным для животных и при вдыхании вызывает ДНК повреждать. [102] Фиолетовый перманганат ион MnO –
4 это печень и почка яд. [111] Употребление более 0,5 г железа может вызвать сердечную недостаточность; такие передозировки чаще всего возникают у детей и могут привести к смерти в течение 24 часов. [102] Карбонил никеля (Ni (CO)4), в количестве 30 частей на миллион, может вызвать дыхательную недостаточность, повреждение мозга и смерть. [102] Выпив грамм или более сульфат меди (CuSO4) может быть фатальным; выжившие могут остаться с серьезным повреждением органов. [112] Более пяти миллиграммов селена очень токсичны; это примерно в десять раз превышает рекомендуемую максимальную суточную дозу в 0,45 миллиграмма; [113] длительное отравление может иметь паралитические эффекты. [102] [n 18]
Другие тяжелые металлы
Некоторые другие несущественные тяжелые металлы имеют одну или несколько токсичных форм. Почечная недостаточность и летальные исходы были зарегистрированы в результате приема диетических добавок германия (всего от 15 до 300 г, потребляемых в течение периода от двух месяцев до трех лет). [102] Воздействие на четырехокись осмия (OsO4) может вызвать необратимое повреждение глаз и привести к дыхательной недостаточности [115] и смерть. [116] Соли индия токсичны при проглатывании более нескольких миллиграммов и влияют на почки, печень и сердце. [117] Цисплатин (PtCl2(NH3)2), который является важным лекарством, используемым для убить раковые клетки, также является ядом почек и нервов. [102] Висмут соединения могут вызвать повреждение печени при приеме в избытке; нерастворимые соединения урана, а также опасные радиация они выделяют, могут вызвать необратимое повреждение почек. [118]
Источники воздействия
Тяжелые металлы могут ухудшать качество воздуха, воды и почвы и впоследствии вызывать проблемы со здоровьем у растений, животных и людей, когда они становятся концентрированными в результате промышленной деятельности. [119] Общие источники тяжелых металлов в этом контексте включают горнодобывающие и промышленные отходы; выбросы транспортных средств; свинцово-кислотные батареи; удобрения; краски; и обработанная древесина; [120] стареющая инфраструктура водоснабжения; [121] и микропластик плавающие в Мировом океане. [122] Недавние примеры загрязнения тяжелыми металлами и рисков для здоровья включают возникновение Болезнь Минаматав Японии (1932–1968; судебные процессы продолжаются с 2016 года); [123] то Катастрофа на плотине Бенту-Родригес в Бразилии, [124] и высокий уровень свинца в питьевой воде, поставляемой жителям Флинт, Штат Мичиган, на северо-востоке США. [125]
Формирование, численность, появление и добыча
Тяжелые металлы до близость железа (в периодической таблице) в основном производятся через звездный нуклеосинтез. В этом процессе более легкие элементы от водорода до кремний пройти последовательный слияние реакции внутри звезд, высвобождая свет и тепло и образуя более тяжелые элементы с более высокими атомными номерами. [129]
Тяжелые тяжелые металлы обычно не образуются таким образом, поскольку реакции синтеза с участием таких ядер будут потреблять, а не выделять энергию. [130] Скорее, они в значительной степени синтезируются (из элементов с более низким атомным номером) посредством захват нейтронов, причем двумя основными режимами этого повторяющегося захвата являются s-процесс и r-процесс. В s-процессе («s» означает «медленный») сингулярные захваты разделены годами или десятилетиями, что позволяет менее стабильным ядрам бета-распад, [131] в то время как в r-процессе («быстром») захваты происходят быстрее, чем ядра могут распадаться. Следовательно, s-процесс идет по более или менее ясному пути: например, стабильные ядра кадмия-110 последовательно бомбардируются свободными нейтронами внутри звезды до тех пор, пока они не образуют ядра кадмия-115, которые являются нестабильными и распадаются с образованием индия-115 (который почти стабильный, с периодом полураспада 30 000 раз старше Вселенной). Эти ядра захватывают нейтроны и образуют нестабильный индий-116, который распадается с образованием олова-116 и т. Д. [129] [132] [n 20] Напротив, в r-процессе такого пути нет. S-процесс останавливается на висмуте из-за короткого периода полураспада следующих двух элементов, полония и астатина, которые распадаются до висмута или свинца. R-процесс настолько быстр, что может пропустить эту зону нестабильности и перейти к созданию более тяжелых элементов, таких как торий и уран. [134]
Тяжелые металлы конденсируются на планетах в результате процессов звездной эволюции и разрушения. Звезды теряют большую часть своей массы, когда она выброшен в конце их жизни, а иногда и после этого в результате нейтронная звезда слияние [135] [n 21] тем самым увеличивая содержание элементов тяжелее гелия в межзвездная среда. Когда гравитационное притяжение заставляет эту материю объединяться и коллапсировать, образуются новые звезды и планеты. [137]
Земная кора состоит примерно из 5% тяжелых металлов по весу, из которых 95% составляет железо. Легкие металлы (
75%) составляют остальные 95% корки. [126] Несмотря на общий дефицит, тяжелые металлы могут концентрироваться в экономически извлекаемых количествах в результате горное строительство, эрозия, или другой геологические процессы. [138]
Тяжелые металлы в основном встречаются в виде литофилы (любящий рок) или халькофилы (рудолюбивый). Литофильные тяжелые металлы — это в основном элементы f-блока и более реактивные из них. d-блок элементы. Они имеют сильное сродство к кислороду и в основном существуют в виде относительно низкой плотности. силикатные минералы. [139] Халькофильные тяжелые металлы — это в основном менее реакционноспособные элементы d-блока, и период 4–6 p-блок металлы и металлоиды. Обычно они встречаются в (нерастворимых) сульфидные минералы. Будучи более плотными, чем литофилы и, следовательно, погружаясь ниже в кору во время ее затвердевания, халькофилы, как правило, менее многочисленны, чем литофилы. [140]
С другой стороны, золото — это сидерофил, или железолюбивый элемент. Он не образует легко соединений ни с кислородом, ни с серой. [141] Во время Формирование Земли, и как наиболее благородный (инертный) металлов, золото погрузилось в основной из-за его склонности к образованию металлических сплавов высокой плотности. Следовательно, это относительно редкий металл. [142] Некоторые другие (менее) благородные тяжелые металлы — молибден, рений, то металлы платиновой группы (рутений, родий, палладий, осмий, иридий, и платина), германий и олово — могут считаться сидерофилами, но только с точки зрения их первичного присутствия на Земле (ядро, мантия и корка), а не корочка. В противном случае эти металлы встречаются в коре в небольших количествах, главным образом в виде халькофилов (в меньшей степени в их родная форма). [143] [n 22]
Концентрации тяжелых металлов под коркой, как правило, выше, причем большинство из них находится в основном в железо-кремний-никелевом ядре. Платина, например, составляет примерно 1 часть на миллиард коры, тогда как его концентрация в ядре считается почти в 6000 раз выше. [144] [145] Недавние предположения предполагают, что уран (и торий) в активной зоне может генерировать значительное количество тепла, которое движет тектоника плит и (в конечном итоге) поддерживает Магнитное поле Земли. [146] [п 23]
Получение тяжелых металлов из их руд — сложная функция от типа руды, химических свойств металлов и экономических аспектов различных методов добычи. В разных странах и на нефтеперерабатывающих заводах могут использоваться разные процессы, в том числе те, которые отличаются от кратких описаний, перечисленных здесь.
Вообще говоря, за некоторыми исключениями, литофильные тяжелые металлы могут быть извлечены из их руд путем электрические или же химическая обработка, а тяжелые халькофильные металлы получают жарка их сульфидные руды с получением соответствующих оксидов, а затем их нагревание для получения сырых металлов. [148] [n 24] Радий встречается в количествах, слишком малых для того, чтобы его можно было экономично добывать, и вместо этого он получается из отработанных ядерное топливо. [151] Халькофильные металлы платиновой группы (МПГ) в основном встречаются в небольших (смешанных) количествах с другими халькофильными рудами. Вовлеченные руды должны быть плавил, жареный, а затем выщелоченный с серная кислота для получения остатка МПГ. Его химически очищают, чтобы получить отдельные металлы в чистом виде. [152] По сравнению с другими металлами МПГ дороги из-за их дефицита. [153] и высокие производственные затраты. [154]
Золото, сидерофил, чаще всего извлекается путем растворения руд, в которых оно находится в цианистый раствор. [155] Золото образует дицианоаурат (I), например: 2 Au + ЧАС2О + ½ O2 + 4 KCN → 2 К [Au (CN)2] + 2 КОН. Цинк добавляется в смесь и, будучи более реактивный чем золото, вытесняет золото: 2 K [Au (CN)2] + Zn → K2[Zn (CN)4] + 2 Au. Золото выпадает в осадок из раствора в виде шлама, отфильтровывается и плавится. [156]
Свойства по сравнению с легкими металлами
Некоторые общие физико-химические свойства легких и тяжелых металлов сведены в таблицу. К сравнению следует относиться с осторожностью, поскольку термины «легкий металл» и «тяжелый металл» не всегда имеют однозначное определение. Также физические свойства твердости и прочности на разрыв могут широко варьироваться в зависимости от чистоты, размером с зернышко и предварительная обработка. [157]
| Физические свойства | Легкие металлы | Тяжелые металлы |
|---|---|---|
| Плотность | Обычно ниже | Обычно выше |
| Твердость [158] | Мягкие, легко режутся или сгибаются | Большинство довольно сложно |
| Тепловое расширение [159] | В основном выше | В основном ниже |
| Температура плавления | В основном низкий [160] | От низкого до очень высокого [161] |
| Предел прочности [162] | В основном ниже | В основном выше |
| Химические свойства | Легкие металлы | Тяжелые металлы |
| Периодическая таблица место расположения | Наиболее часто встречается в группах 1 и 2 [163] | Почти все найдено в группах 3 через 16 |
| Изобилие в земной коре [126] [164] | Более обильный | Менее обильный |
| Основное появление (или источник) | Литофилы [128] | Литофилы или халькофилы (Au это сидерофил) |
| Реактивность [77] [164] | Более реактивный | Менее реактивный |
| Сульфиды | От растворимого до нерастворимого [n 25] | Чрезвычайно нерастворим [169] |
| Гидроксиды | От растворимого до нерастворимого [n 26] | Обычно нерастворим [173] |
| Соли [166] | В основном образуют бесцветные растворы в воде. | В основном образуют цветные растворы в воде. |
| Комплексы | В основном бесцветный [174] | В основном цветные [175] |
| Биологическая роль [176] | Включают макроэлементы (Na, Mg, K, Ca) | Включают микроэлементы (V, Cr, Mn, Fe, Co, Ni, Cu, Zn, Пн) |
Эти свойства позволяют относительно легко отличить легкий металл, такой как натрий, от тяжелого металла, такого как вольфрам, но различия становятся менее четкими на границах. Легкие структурные металлы, такие как бериллий, скандий и титан, обладают некоторыми характеристиками тяжелых металлов, например более высокими температурами плавления; [n 27] постпереходные тяжелые металлы, такие как цинк, кадмий и свинец, обладают некоторыми характеристиками легких металлов, такими как относительно мягкость, более низкие температуры плавления, [n 28] и образуя преимущественно бесцветные комплексы. [21] [23] [24]
Использует
Тяжелые металлы присутствуют практически во всех аспектах современной жизни. Железо может быть наиболее распространенным, поскольку на него приходится 90% всех очищенных металлов. Платина может быть наиболее распространенной, поскольку считается, что она содержится в 20% всех потребительских товаров или используется для ее производства. [181]
Некоторые распространенные виды использования тяжелых металлов зависят от общих характеристик металлов, таких как электрическая проводимость и отражательная способность или общие характеристики тяжелых металлов, такие как плотность, прочность и долговечность. Другое использование зависит от характеристик конкретного элемента, например, от их биологической роли в качестве питательных веществ или ядов или некоторых других конкретных атомных свойств. Примеры таких атомарных свойств включают: частично заполненный d- или же f-орбитали (во многих переходных, лантаноидных и актинидных тяжелых металлах), которые делают возможным образование окрашенных соединений; [182] емкость большинства ионов тяжелых металлов (таких как платина, [183] церий [184] или висмут [185] ) существовать в разных состояния окисления и поэтому действуют как катализаторы; [186] плохо перекрывающиеся 3d или 4f орбитали (в железе, кобальте и никеле или тяжелых металлах лантаноидов из европий через тулий), вызывающие магнитные эффекты; [187] и высокие атомные номера и электронные плотности которые лежат в основе их приложений в ядерной науке. [188] Типичные виды использования тяжелых металлов можно в общих чертах разделить на следующие шесть категорий. [189] [n 29]
В зависимости от веса или плотности

Некоторые виды использования тяжелых металлов, в том числе в спорте, машиностроение, боеприпасы, и ядерная наука, воспользуйтесь их относительно высокой плотностью. В подводное плавание, свинец используется как балласт; [191] в скачки для инвалидов каждая лошадь должна иметь определенный вес свинца, основанный на факторах, включая прошлые выступления, чтобы уравнять шансы различных участников. [192] В гольф, вольфрам, латунь, или медные вставки в фарватер дубинки и утюги понизить центр тяжести клюшки, чтобы мяч легче поднялся в воздух; [193] Мячи для гольфа с вольфрамовым сердечником обладают лучшими летными характеристиками. [194] В нахлыст, тонущие шнуры имеют ПВХ покрытие залито порошком вольфрама, так что они тонут с необходимой скоростью. [195] В легкая атлетика спорт стали шары, используемые в метание молота и толкание ядра события заполняются свинцом для достижения минимального веса, требуемого международными правилами. [196] Вольфрам использовался в шарах для метания молотов по крайней мере до 1980 г .; минимальный размер шара был увеличен в 1981 году, чтобы исключить необходимость в том, что в то время было дорогим металлом (в три раза дороже других молотов), доступным не во всех странах. [197] Вольфрамовые молоты были настолько плотными, что слишком глубоко проникали в дерн. [198]
В машиностроении тяжелые металлы используются для балласта лодок, [199] самолеты [200] и автотранспортные средства; [201] или в балансиры на колесах и коленчатые валы, [202] гироскопы, и пропеллеры, [203] и центробежные муфты, [204] в ситуациях, требующих максимального веса в минимальном пространстве (например, в смотреть движения). [200]
А. М. Рассел и К. Л. Ли
Отношения структура – собственность
в цветных металлах (2005, стр.16)
В военных боеприпасах вольфрам или уран используются в броня [205] и бронебойные снаряды, [206] а также в ядерное оружие для повышения эффективности (путем отражающие нейтроны и на мгновение задерживая расширение реагирующих материалов). [207] В 1970-е годы тантал оказался более эффективным, чем медь, в кумулятивный заряд и взрывоопасное противотанковое оружие из-за его более высокой плотности, что обеспечивает большую концентрацию усилий и лучшую деформируемость. [208] Меньше-токсичные тяжелые металлы, такие как медь, олово, вольфрам и висмут, и, вероятно, марганец (а также бор, металлоид), заменили свинец и сурьму в зеленые пули используется некоторыми армиями и в некоторых боеприпасах для развлекательной стрельбы. [209] Высказывались сомнения в безопасности (или зеленые полномочия) вольфрама. [210]
Поскольку более плотные материалы поглощают больше радиоактивных выбросов, чем более легкие, тяжелые металлы полезны для радиационная защита и чтобы фокусировать пучки излучения в линейные ускорители и лучевая терапия Приложения. [211]
На основе прочности или долговечности

Прочность или долговечность тяжелых металлов, таких как хром, железо, никель, медь, цинк, молибден, олово, вольфрам и свинец, а также их сплавов, делает их полезными для изготовления артефактов, таких как инструменты, оборудование, [214] бытовая техника, [215] посуда, [216] трубы [215] железнодорожные пути, [217] здания [218] и мосты, [219] автомобили, [215] замки, [220] мебель, [221] корабли [199] самолеты [222] чеканка [223] и ювелирные изделия. [224] Они также используются в качестве легирующих добавок для улучшения свойств других металлов. [n 31] Из двух десятков элементов, которые использовались в монетизированной мировой чеканке монет, только два, углерод и алюминий, не являются тяжелыми металлами. [226] [n 32] Золото, серебро и платина используются в ювелирных изделиях. [n 33] как (например) никель, медь, индий и кобальт в цветное золото. [229] Недорогие украшения и детские игрушки в значительной степени могут состоять из тяжелых металлов, таких как хром, никель, кадмий или свинец. [230]
Медь, цинк, олово и свинец механически более слабые, но полезные коррозия профилактические свойства. Пока каждый из них будет реагировать с воздухом, в результате патины либо различных солей меди, [231] карбонат цинка, оксид олова, или смесь оксид свинца, карбонат, и сульфат, дарят ценные защитные свойства. [232] Поэтому медь и свинец используются, например, в качестве кровельные материалы; [233] [n 34] цинк действует как антикоррозийный агент в оцинкованная сталь; [234] и олово служит той же цели на стальные банки. [235]
Технологичность и коррозионная стойкость железа и хрома повышаются за счет добавления гадолиний; то сопротивление ползучести никеля улучшается с добавлением тория. В медь добавляют теллур (Теллур Медь) и стальных сплавов для улучшения их обрабатываемости; и сделать его более твердым и кислотостойким. [236]
Биологические и химические

В биоцидный эффекты некоторые тяжелые металлы известны с глубокой древности. [238] Платина, осмий, медь, рутений и другие тяжелые металлы, включая мышьяк, используются в противораковых препаратах или показали потенциал. [239] Сурьма (антипротозойная), висмут (противоязвенный), золото (антиартритический) и железо (противомалярийный) также важны в медицине. [240] Медь, цинк, серебро, золото или ртуть используются в антисептик составы; [241] небольшие количества некоторых тяжелых металлов используются для контроля роста водорослей, например, в градирни. [242] В зависимости от их предполагаемого использования в качестве удобрений или биоцидов, агрохимикаты может содержать тяжелые металлы, такие как хром, кобальт, никель, медь, цинк, мышьяк, кадмий, ртуть или свинец. [243]
Отдельные тяжелые металлы используются в качестве катализаторов при переработке топлива (например, рений), синтетическая резина и производство волокна (висмут), устройства контроля выбросов (палладий), а в самоочищающиеся печи (куда оксид церия (IV) в стенках таких духовок помогает окислять углеродостатки готовки). [244] В химии мыла тяжелые металлы образуют нерастворимое мыло, которое используется в консистентные смазки, сушилки для краски и фунгициды (кроме лития, щелочных металлов и аммоний растворимые мыла в ионной форме). [245]
Расцветка и оптика
Цвета стекло, керамические глазури, краски, пигменты, и пластмассы обычно производятся путем включения тяжелых металлов (или их соединений), таких как хром, марганец, кобальт, медь, цинк, селен, цирконий, молибден, серебро, олово, празеодим, неодим, эрбий, вольфрам, иридий, золото, свинец или уран. [247] Татуировка чернила могут содержать тяжелые металлы, такие как хром, кобальт, никель и медь. [248] Высокая отражательная способность некоторых тяжелых металлов важна при строительстве зеркала, включая точность астрономические инструменты. Отражатели фар основаны на превосходной отражательной способности тонкой пленки родия. [249]
Электроника, магниты и освещение

Тяжелые металлы или их соединения можно найти в электронные компоненты, электроды, и проводка и солнечные панели где они могут использоваться как проводники, полупроводники или изоляторы. Молибденовый порошок используется в печатная плата чернила. [250] Оксид рутения (IV) титан с покрытием аноды используются для промышленного производства хлор. [251] Домашние электрические системы по большей части имеют медный провод из-за его хороших проводящих свойств. [252] Серебро и золото используются в электрических и электронных устройствах, особенно при контакте. переключателив результате их высокой электропроводности и способности противостоять или минимизировать образование загрязнений на своей поверхности. [253] Полупроводники теллурид кадмия и арсенид галлия используются для изготовления солнечных батарей. Оксид гафния, изолятор, используется как регулятор напряжения в микрочипы; оксид тантала, другой изолятор, используется в конденсаторы в мобильные телефоны. [254] Тяжелые металлы используются в аккумуляторах более 200 лет, по крайней мере, с тех пор, как Вольта изобрел медь и серебро гальваническая свая в 1800 г. [255] Прометий, лантан, и ртуть — другие примеры, найденные соответственно в атомный, никель-металлогидрид, и кнопочная ячейка батареи. [256]
Магниты изготовлены из тяжелых металлов, таких как марганец, железо, кобальт, никель, ниобий, висмут, празеодим, неодим, гадолиний и диспрозий. Неодимовые магниты — самый сильный тип постоянный магнит в продаже. Они являются ключевыми компонентами, например, дверных замков автомобилей, стартеры, топливные насосы, и электрические стеклоподъемники. [257]
Тяжелые металлы используются в освещение, лазеры, и светодиоды (Светодиоды). Плоские дисплеи включать тонкую пленку электропроводящего оксид индия и олова. Флуоресцентное освещение в своей работе полагается на пары ртути. Рубиновые лазеры генерировать темно-красные лучи, возбуждая атомы хрома; лантаноиды также широко используются в лазерах. Галлий, индий и мышьяк; [258] а медь, иридий и платина используются в светодиодах (последние три в органические светодиоды). [259]
Ядерная

Нишевые применения тяжелых металлов с высокими атомными номерами встречаются в диагностическая визуализация, электронная микроскопия, и ядерная наука. В диагностической визуализации тяжелые металлы, такие как кобальт или вольфрам, составляют анодные материалы, обнаруженные в рентгеновские трубки. [263] В электронной микроскопии тяжелые металлы, такие как свинец, золото, палладий, платина или уран, используются для создания проводящих покрытий и для введения электронной плотности в биологические образцы путем окрашивание, отрицательное окрашивание, или же вакуумное напыление. [264] В ядерной науке ядра тяжелых металлов, таких как хром, железо или цинк, иногда стреляют по другим мишеням из тяжелых металлов для получения сверхтяжелые элементы; [265] тяжелые металлы также используются как раскол цели по производству нейтроны [266] или же радиоизотопы такие как астат (используя в последнем случае свинец, висмут, торий или уран). [267]
Источник https://elton-zoloto.ru/metally-i-splavy/chto-otnositsja-k-tjazhelym-metallam.html
Источник https://wikidea.ru/wiki/Heavy_metals
Источник



