Содержание
Взаимодействие кислот с металлами. Взаимодействие серной кислоты с металлами
Химическая реакция кислоты с металлом является специфичной для данных классов соединений. В ее ходе протон водорода восстанавливается и в связке с кислотным анионом заменяется на катион металла. Это пример реакции с образованием соли, хотя существует и несколько типов взаимодействий, не подчиняющихся данному принципу. Они протекают как окислительно-восстановительные и не сопровождаются выделением водорода.
Принципы реакций кислот с металлами
Все реакции неорганической кислоты с металлом приводят к образованию солей. Исключением является, пожалуй, лишь реакция благородного металла с царской водкой, смесью соляной и азотной кислоты. Любое другое взаимодействие кислот с металлами приводит к образованию соли. В случае если кислота не является ни серной концентрированной, ни азотной, то в качестве продукта выщепляется молекулярный водород.
Но когда в реакцию вступает концентрированная серная кислота, взаимодействие с металлами протекает по принципу окислительно-восстановительного процесса. Потому экспериментально было выделено два типа взаимодействий типичных металлов и крепких неорганических кислот:
- взаимодействие металлов с разбавленными кислотами;
- взаимодействие с концентрированной кислотой.
Реакции по первому типу протекают с любой кислотой. Исключением является лишь концентрированная серная кислота и азотная кислота любой концентрации. Они реагируют по второму типу и приводят к образованию солей и продуктов восстановления серы и азота.
Типичные взаимодействие кислот с металлами
Металлы, расположенные левее водорода в стандартном электрохимическом ряду, реагируют с разбавленной серной кислотой и другими кислотами различной концентрации за исключением азотной с образованием соли и выделением молекулярного водорода. Металлы, расположенные правее водорода в ряду электроотрицательности, не могут реагировать с указанными выше кислотами и взаимодействуют лишь с азотной кислотой независимо от ее концентрации, с концентрированной серной кислотой и с царской водкой. Это типичное взаимодействие кислот с металлами.
Реакции металлов с концентрированной серной кислотой
При содержании серной кислоты в растворе более 68%, она считается концентрированной и взаимодействует с металлами левее и правее водорода. Принцип протекания реакции с металлами различной активности показан на фото ниже. Здесь окислителем является атом серы в сульфат-анионе. Она восстанавливается до сероводорода, 4-валентного оксида или до молекулярной серы.

Реакции с разбавленной азотной кислотой
Разбавленная азотная кислота реагирует с металлами, расположенными левее и правее водорода. В ходе реакции с активными металлами образуется аммиак, который сразу же растворяется и взаимодействует с нитрат-анионом, образуя еще одну соль. С металлами средней активности кислота реагирует с выделением молекулярного азота. С малоактивными реакция протекает с выделением оксида 2-валентного азота. Чаще всего образуется несколько продуктов восстановления серы в одной реакции. Примеры реакций предложены в графическом приложении ниже.

Реакции с концентрированной азотной кислотой
В данном случае окислителем также выступает азот. Все реакции заканчиваются образованием соли и выделением оксида азота. Схемы протекания окислительно-восстановительных реакций предложены на графическом приложении. При этом отдельного внимания заслуживает реакция царской водки с малоактивными элементами. Такое взаимодействие кислот с металлами неспецифично.

Реакционная способность металлов
Металлы вступают в реакции с кислотами достаточно охотно, хотя есть несколько инертных веществ. Это благородные металлы и элементы, имеющие высокий стандартный электрохимический потенциал. Существует ряд металлов, который построен на основании данного показателя. Он называется рядом электроотрицательности. Если металл стоит в нем левее водорода, то он способен вступать в реакцию с разбавленной кислотой.
Существует лишь одно исключение: железо и алюминий за счет образования на их поверхности 3-валентных оксидов не могут реагировать с кислотой без нагревания. Если смесь подогревается, то изначально в реакцию вступает оксидная пленка металла, а затем он сам растворяется в кислоте. Металлы, расположенные правее водорода в электрохимическом ряду активности, не могут реагировать с неорганической кислотой, в том числе и с разбавленной серной. Исключений из правил два: эти металлы растворяются в концентрированной и разбавленной азотной кислоте и царской водке. В последней не могут быть растворены только родий, рутений, иридий и осмий.
С какими веществами реагирует золото, какие у него свойства?
Что реагирует на золото и какие вещества помогут распознать металл в обычных условиях или в лаборатории? Это сложный вопрос, поскольку по своей сути это элемент периодической таблицы Менделеева, который отличается инертностью.

Растворение золота в царской водке
Инертность — способность вещества не реагировать на кислоты, щелочи и не окисляться при контакте с воздухом и водой. В таблице металл обозначается символом Au, а «золото» с латыни переводится, как «восход солнца». Золото и платина как раз стали называться благородными металлами, когда выяснилась их способность не реагировать на внешние факторы и химические реагенты. Но химия, как и любая другая наука, не стоит на месте, и удалось обнаружить несколько веществ, которые вступают с Au в реакцию.
Свойства металла
Химические свойства золота свидетельствуют о том, что этот металл все же может реагировать на некоторые вещества.
Так с чем же взаимодействует Au и при каких условиях?
- Ртуть может образовывать с золотом особое соединение — амальгаму. Это сплав двух металлов, молекулы ртути притягивают к себе молекулы Au, в результате чего образуется соединение.
- Золото растворяется в царской водке, об этом известно довольно давно, но смесь высокой концентрации азотной и соляной кислот не имеет аналогов. Химики используют ее до сих пор, они не нашли царской водке достойной замены и применяют ее при проведении аффинажа.
- Реакция селеновой кислоты и Au начинается только тогда, когда концентрированную кислоту разогревают до определенной температуры.
- Еще благородный металл вступает в реакцию с йодистым калием. Но в некоторых случаях для идентификации используют обычный раствор йода на спирту, который присутствует в аптечке.
- Жидкий бром и вода с цианидами — вот еще два химических реагента, которые способны вступить в реакцию с Au.
Способности ртутит притягивать молекулы Au известны давно. В старину это свойство металла использовали для добычи золота. Были созданы специальные шлюзы, поверхность которых покрывалась слоем ртути, притягивавшей Au и позволявшей увеличить уровень его добычи. Минусом такого способа считалась токсичность, человек, который имел постоянный контакт со ртутью, жертвовал своим здоровьем, добывая золото.
Амальгама — состояние обратимое, чтобы Au вновь приобрел свой первоначальный вид, смесь необходимо подогреть примерно до 800 градусов.
Задолго до того как Дмитрию Менделееву приснилась его периодическая таблица, алхимикам была известна способность золота растворяться в смеси двух кислот. Азотную и соляную кислоты смешивали и использовали для проведения различных опытов. Ученые того времени шифровали свои записи, по этой причине не расписывали реакцию, а рисовали ее.
Алхимики изображали льва, который поглощал солнце, животное стояло на задних лапах и поедало желтый круг. Золото ассоциировалось с солнцем за свой цвет, а вот львом была как раз смесь двух кислот. Царская водка, по сути, — универсальный растворитель, которому под силу разложить на молекулы все благородные металлы. Смесь кислот используют и сегодня, при проведении аффинажа или других опытов. Формула царской водки: HNO3+3 HCl.

Реакция золота на йод
Такая смесь способна растворить даже платину и большинство существующих металлов. Только серебро не слишком охотно растворяется в смеси двух кислот. Но с течением времени сила растворителя уменьшается: чем больше реагент контактирует с воздухом, тем слабее он становится.
Реакция с селеновой кислотой проходит при определенных условиях. Чтобы растворить золото, необходимо использовать концентрированную кислоту, нагреть ее до определенной температуры и при этом обеспечить приток кислорода. Если кислорода будет недостаточно, то реакция будет идти медленно.
Йодистый калий используют довольно редко в химии, подобным образом Au идентифицировать не любят. Зато в обычной жизни украшения, изготовленные из золота, часто проверяют на подлинность, используя раствор йода на спирту.
Если говорить о применении в промышленных масштабах, то способность цианидов взаимодействовать с желтым металлом нашла свое место в этой отрасли. Цианирование — один из методов очистки золота, он помогает отделить Au от частиц породы и примесей.
Несмотря на инертность, при работе с Au стоит учитывать один факт. Если металл с другими реагентами нагреть, то реакция пойдет быстрее. Но золото очень быстро возвращается в первичное состояние, что нужно иметь в виду.
Список веществ, которые способны вступать в реакцию с благородным металлом, на этом исчерпан. Золото не растворяется в воде, в спирте и других веществах. Реагенты не способны нанести металлу вред, разложить его на молекулы, но не стоит забывать, что чистое золото встречается только в слитках. Даже в природе этот металл имеет примеси, которые значительно снижают его инертность.
Оценив все свойства Au, ученые пришли к выводу, что элемент на нашей планете появился из космоса. Золото попало на Землю с частицами космических тел и метеоритов. На нашей планете не существовало условий, благоприятных для его формирования.
Химические свойства элемента под номером 79 немногочисленны, но они все же помогают химикам проводить опыты и исследования, делать очередные открытия. Но не только химия помогает идентифицировать благородный металл, есть и другая наука, которая в этом неплохо преуспела.
Физические показатели
Наряду с химическими, у золота есть и физические свойства, к которым относят:
- Невысокую твердость, по шкале Мооса от 2,5 до 3 единиц.
- Пластичность и ковкость.
- Желтый цвет.
Au не обладает высокой твердостью. В то время как алмазу присваивают 9 баллов по шкале Мооса, этот элемент удостоился всего 3. Чтобы повысить твердость Au, его сплавляют с другими металлами, в результате чего возникает лигатура, используемая для создания украшений. Драгоценности из чистого золота практически не встречаются, они тяжелые и легко деформируются при носке.
Для того чтобы идентифицировать металл, достаточно попробовать его на зуб. Можно укусить изделие, если оно легко поддается деформации и меняет форму, на поверхности остаются следы от зубов, то можно не сомневаться в его подлинности.
Au отличается ковкостью и пластичностью. Можно разрезать слиток ножом, не прилагая особых усилий, а также превратить кусок благородного металла в тонкий лист. Благодаря этому создают сусальное золото, которое используют в качестве декоративного материала: им покрывают купола церквей, защищая их от воздействия факторов окружающей среды.
Золото — единственный металл, который обладает желтым цветом. Этот оттенок повлиял на характеристики элемента, его ассоциировали с силой солнца. Металлу присваивали различные свойства, теплый оттенок свидетельствовал и о таинственном происхождении элемента.
Испокон веков Au ассоциируется у людей с богатством, высоким положением в обществе. В старину обычным людям не дозволялось носить золотые украшения, поскольку этой прерогативы были достойны только представители высшего общества.
Сферы применения
Благодаря своим свойствам, красоте и инертности Au нашел применение в различных отраслях промышленности и не только.
Его используют сегодня:
- в ювелирной промышленности;
- в косметологии и медицине;
- для создания электроники;
- в космической отрасли.
Естественно, что наибольшая часть благородного металла идет для создания произведений ювелирной промышленности. Из него делают украшения, инкрустируя их драгоценными и полудрагоценными камнями. Кроме того, золото в слитках используется как материал для инвестиций, в них вкладывают деньги, и это неизменно приносит прибыль.
Большое количество средств по уходу за кожей содержит в своем составе Au. Этот элемент помогает справиться с признаками старения, в пример можно привести нити из золота, которые вживляют в кожу и которые оказывают омолаживающее действие на организм. Еще металл используют при лечении заболеваний суставов (артритов), а также с его помощью лечат аутоиммунные и онкологические заболевания. Специальную сыворотку, в составе которой есть Au, вводят в организм больного.
Содержат Au в небольшом количестве контакты материнских плат компьютеров и мобильных телефонов, их покрывают золотом.
Если говорить о космической промышленности, то тут элемент используют везде, где необходимы его антикоррозийные свойства. Золотом покрывают стекла шаттлов и шлемов космонавтов. А также некоторые части контактов при изготовлении космических кораблей.
Золото — самый популярный металл на планете, его добыча ведется так давно, что сложно определить дату, когда именно человечество познакомилось с Au. Но точно можно сказать, что произошло это еще задолго до нашей эры. С годами популярность Au только растет, цена на металл поднимается, размеры добычи падают, но любовь человечества к золоту не снижается. Ему присваивают магические свойства, наделяют энергией солнца и называют то металлом Бога, то дьявола.
Причиной «особого отношения» к золоту является не только его красота, но и свойства, которые делают металл благородным и столь ценным для человека.
14 различных типов металлов

Термин «металл» происходит от греческого слова «metalléuō», что означает выкапываю или добываю из земли. Наша планета содержит много металла. На самом деле из 118 элементов периодической системы порядка 95 являются металлами.
Это число не является точным, потому что граница между металлами и неметаллами довольно расплывчата: нет стандартного определения металлоида, как нет и полного согласия относительно элементов, соответствующим образом классифицированных как таковые.
Сегодня мы используем различные виды металлов, даже не замечая их. Начиная с зажимов в сантехнике и заканчивая устройством, которое вы используете для чтения этой статьи, все они сделаны из определенных металлов. Фактически, некоторые металлические элементы необходимы для биологических функций, таких как приток кислорода и передача нервных импульсов. Некоторые из них также широко используются в медицине в виде антацидов.
Все металлы в периодической таблице можно классифицировать по их химическим или физическим свойствам. Ниже мы перечислили некоторые различные типы металлов вместе с их реальным применением.
Классификация по физическим свойствам
14. Легкие металлы

Сплав титана 6AL-4V
Примеры: Алюминий, титан, магний
Легкие металлы имеют относительно низкую плотность. Формального определения или критериев для идентификации этих металлов нет, но твердые элементы с плотностью ниже 5 г/см³ обычно считаются легкими металлами.
Металлургия легких металлов была впервые развита в середине 19 века. Хотя большинство из них происходит естественным путем, значительная их часть образуется при электротермии и электролизе плавленых солей.
Их сплавы широко используются в авиационной промышленности благодаря их низкой плотности и достаточным механическим свойствам. Например, сплав титана 6AL-4V составляет почти 50 процентов всех сплавов, используемых в авиастроении. Он используется для изготовления роторов, лопастей компрессоров, мотогондол, компонентов гидравлических систем.
13. Тяжелые металлы

Окисленные свинцовые конкреции и кубик размером 1 см3
Примеры: железо, медь, кобальт, галлий, олово, золото, платина.
Тяжелые металлы — это элементы с относительно высокой плотностью (обычно более 5 г/см³) и атомным весом. Они, как правило, менее реактивны и содержат гораздо меньше растворимых сульфидов и гидроксидов, чем более легкие металлы.
Эти металлы редки в земной коре, но они присутствуют в различных аспектах современной жизни. Они используются в солнечных батареях, сотовых телефонах, транспортных средствах, антисептиках и ускорителях частиц.
Тяжелые металлы часто смешиваются в окружающей среде из-за промышленной деятельности, ухудшая качество почвы, воды и воздуха, а затем вызывая проблемы со здоровьем у животных и растений. Выбросы транспортных средств, горнодобывающие и промышленные отходы, удобрения, свинцово-кислотные батареи и микропластики, плавающие в океанах, являются одними из наиболее распространенных источников тяжелых металлов в этом контексте.
12. Белый металл

Подшипники из белого металла
Примеры: Обычно изготавливается из олова, свинца, висмута, сурьмы, кадмия, цинка.
Белые металлы — это различные светлые сплавы, используемые в качестве основы для украшений или изделий из серебра. Например, многие сплавы на основе олова или свинца используются в ювелирных изделиях и подшипниках.
Белый металлический сплав изготавливается путем объединения определенных металлов в фиксированных пропорциях в соответствии с требованиями конечного продукта. Основной металл для ювелирных изделий, например, формуется, охлаждается, экстрагируется, а затем полируется, чтобы придать ему точную форму и блестящий вид.
Они также используются для изготовления тяжелых подшипников общего назначения, подшипников внутреннего сгорания среднего размера и электрических машин.
11. Хрупкий металл

Хрупкое разрушение чугуна
Примеры: сплавы углеродистой стали, чугуна и инструментальной стали.
Металл считается хрупким, если он твердый, но не может противостоять ударам или вибрации под нагрузкой. Такие металлы под воздействием напряжения ломаются без заметной пластической деформации. Они имеют низкую прочность на разрыв и часто издают щелкающий звук при поломке.
Многие стальные сплавы становятся хрупкими при низких температурах, в зависимости от их обработки и состава. Чугун, например, твердый, но хрупкий из-за высокого содержания углерода. Напротив, керамика и стекло гораздо более хрупки, чем металлы, из-за их ионных связей.
Галлий, висмут, хром, марганец и бериллий также хрупки. Они часто используются в различных гражданских и военных целях, связанных с высокими деформационными нагрузками. Чугун, устойчивый к повреждениям в результате окисления, используется в машинах, трубах и деталях автомобильной промышленности, таких как корпуса коробок передач и головки цилиндров.
10. Тугоплавкий металл
Микроскопическое изображение вольфрамовой нити в лампе накаливания
Примеры: молибден, вольфрам, тантал, рений, ниобий.
Тугоплавкие металлы имеют чрезвычайно высокие температуры плавления (более 2000 °С) и устойчивы к износу, деформации и коррозии. Они являются хорошими проводниками тепла и электричества и имеют высокую плотность.
Другой ключевой характеристикой является их термостойкость: они не расширяются и не растрескиваются при многократном нагревании и охлаждении. Однако они могут деформироваться при высоких нагрузках и окисляться при высоких температурах.
Благодаря своей прочности и твердости они идеально подходят для сверления и резки. Карбиды и сплавы тугоплавких металлов используются почти во всех отраслях промышленности, включая горнодобывающую, автомобильную, аэрокосмическую, химическую и ядерную.
Металлический вольфрам, например, используется в ламповых нитях. Сплавы рения используются в гироскопах и ядерных реакторах. А ниобиевые сплавы используются для форсунок жидкостных ракетных двигателей.
9. Черные и цветные металлы

Валы-шестерни из (черной) нержавеющей стали
Черные металлы: Сталь, чугун, сплавы железа.
Цветные металлы: Медь, алюминий, свинец, цинк, серебро, золото.
Термин «железо» происходит от латинского слова «Ferrum», что переводится как «железо». Таким образом, термин «черный металл» обычно означает «содержащий железо», тогда как «цветной металл» означает металлы и сплавы, которые не содержат достаточного количества железа.
Поскольку черные металлы могут иметь широкий спектр легирующих элементов, которые значительно изменяют их характеристики, очень трудно поместить свойства всех черных металлов под один зонт. Тем не менее некоторые обобщения могут быть сделаны, например, большинство черных металлов являются твердыми и магнитными.
Черные металлы используются для применения с высокой нагрузкой и низкой скоростью, в то время как цветные металлы предпочтительны для применения с высокой скоростью и нулевой нагрузкой для применения с низкой нагрузкой.
Сталь является наиболее распространенным черным металлом. Она составляет около 80% всего металлического материала благодаря своей доступности, высокой прочности, низкой стоимости, простоте изготовления и широкому спектру свойств. Она широко используется в строительстве и обрабатывающей промышленности. Фактически, рост производства стали показывает общее развитие промышленного мира.
8. Цветные и благородные металлы

Ассортимент благородных металлов
Цветные металлы: медь, алюминий, олово, никель, цинк
Благородные металлы: родий, ртуть, серебро, рутений, осмий, иридий
Цветные металлы — это обычные и недорогие металлы, которые корродируют, окисляются или тускнеют быстрее, чем другие металлы, когда подвергаются воздействию воздуха или влаги. Они в изобилии встречаются в природе и легко добываются.
Они широко используются в промышленных и коммерческих целях и имеют неоценимое значение для мировой экономики благодаря своей полезности и повсеместности. Некоторые цветные металлы обладают отличительными характеристиками, которые не могут быть продублированы другими металлами. Например, цинк используется для гальванизации стали, чтобы защитить ее от коррозии, а никель — для изготовления нержавеющей стали.
Благородные металлы, с другой стороны, устойчивы к окислению и коррозии во влажном воздухе. Согласно атомной физике, благородные металлы имеют заполненный электрон d-диапазона. В соответствии с этим строгим определением, медь, серебро и золото являются благородными металлами.
Они находят применение в таких областях, как орнамент, металлургия и высокие технологии. Их точное использование варьируется от одного элемента к другому. Некоторые благородные металлы, такие как родий, используются в качестве катализаторов в химической и автомобильной промышленности.
7. Драгоценные металлы

Родий: 1 грамм порошка, 1 грамм прессованного цилиндра и 1 г аргонодуговой переплавленной гранулы
Примеры: палладий, золото, платина, серебро, родий.
Драгоценные металлы считаются редкими и имеют высокую экономическую ценность. Химически они менее реакционноспособны, чем большинство элементов (включая благородные металлы). Они также пластичны и имеют высокий блеск.
Несколько веков назад эти металлы использовались в качестве валюты. Но сейчас они в основном рассматриваются как промышленные товары и инвестиции. Многие инвесторы покупают драгоценные металлы (в основном золото), чтобы диверсифицировать свои портфели или победить инфляцию.
Серебро — второй по популярности драгоценный металл для ювелирных изделий (после золота). Однако его значение выходит далеко за рамки красоты. Оно обладает исключительно высокой тепло- и электропроводностью и чрезвычайно низким контактным сопротивлением. Именно поэтому серебро широко используется в электронике, батареях и противомикробных препаратах.
Классификация по химическим свойствам
6. Щелочные металлы

Твердый металлический натрий
Примеры: натрий, калий, рубидий, литий, цезий и франций.
Щелочь относится к основной природе гидроксидов металлов. Когда эти металлы реагируют с водой, они образуют сильные основания, которые легко нейтрализуют кислоты.
Они настолько реактивны, что обычно встречаются в природе в слиянии с другими веществами. Карналлит (хлорид калия-магния) и сильвин (хлорид калия), например, растворимы в воде и, таким образом, легко извлекаются и очищаются. Нерастворимые в воде щелочи, такие, как фторид лития, также существуют в земной коре.
Одно из самых популярных применений щелочных металлов — использование цезия и рубидия в атомных часах, наиболее точных из известных эталонов времени и частоты. Литий используется в качестве анода в литиевых батареях, композиты калия используются в качестве удобрений, а ионы рубидия используются в фиолетовых фейерверках. Чистый металлический натрий широко используется в натриевых лампах, которые очень эффективно излучают свет.
5. Щелочноземельные металлы

Изумрудный кристалл, основной минерал бериллия.
Примеры: бериллий, кальций, магний, барий, стронций и радий.
Щелочноземельные металлы в стандартных условиях мягкие и серебристо-белые. Они имеют низкую плотность, температуру кипения и температуру плавления. Хотя они не так реакционноспособны, как щелочные металлы, они очень легко образуют связи с элементами. Как правило, они вступают в реакцию с галогенами, образуя галогениды щелочноземельных металлов.
Все они встречаются в земной коре, кроме радия, который является радиоактивным элементом. Радий уже распадался в ранней истории Земли из-за относительно короткого периода полураспада (1600 лет). Современные образцы поступают из цепочки распада урана и тория.
Щелочноземельные металлы имеют широкий спектр применения. Бериллий, например, используется в полупроводниках, теплопроводниках, электрических изоляторах и в военных целях. Магний часто сплавляют с цинком или алюминием для получения материалов со специфическими свойствами. Кальций в основном используется в качестве восстановителя, а барий используется в вакуумных трубках для удаления газов.
4. Переходные металлы
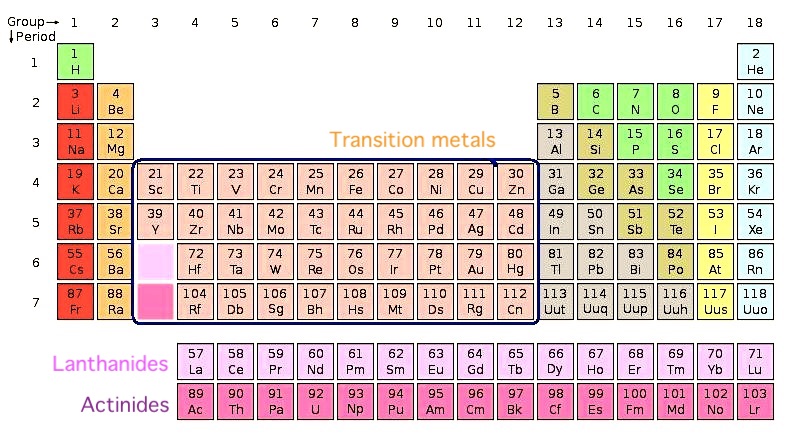
Примеры: титан, ванадий, хром, никель, серебро, вольфрам, платина, кобальт.
Большинство элементов используют электроны из своей внешней оболочки для связи с другими элементами. Переходные металлы, однако, могут использовать две крайние оболочки для соединения с другими элементами. Это химическая особенность, которая позволяет им связываться со многими различными элементами в различных формах.
Они занимают среднюю часть таблицы Менделеева, служа мостом между (или переходом) между двумя сторонами таблицы. Более конкретно, есть 38 переходных металлов в группах с 3 по 12 периодической таблицы. Все они являются пластичными, податливыми и хорошими проводниками тепла и электричества.
Многие из этих металлов, такие как медь, никель, железо и титан, используются в конструкциях и в электронике. Большинство из них образуют полезные сплавы друг с другом и с другими металлическими веществами. Некоторые из них, включая золото, серебро и платину, называются благородными металлами, потому что они крайне инертны и устойчивы к кислотам.
3. Постпереходные металлы

Висмут в виде синтетических кристаллов
Примеры: алюминий, галлий, олово, свинец, таллий, индий, висмут.
Постпереходные металлы в периодической таблице — это элементы, расположенные справа от переходных металлов и слева от металлоидов. Из-за своих свойств они также называются «бедными» или «другими» металлами.
Физически они хрупки (или мягки) и имеют более низкую температуру плавления и механическую прочность, чем переходные металлы. Их кристаллическая структура довольно сложна: они проявляют ковалентные или направленные эффекты связи.
Различные металлы этого семейства имеют различное применение. Алюминий, например, используется для изготовления оконных рам, кухонной посуды, банок, фольги, деталей автомобилей. Оловянные сплавы используются в мягких припоях, оловянных и сверхпроводящих магнитах.
Индиевые сплавы используются для изготовления плоских дисплеев и сенсорных экранов, а галлий — в топливных элементах и полупроводниках.
2. Лантаноиды

1-сантиметровый кусок чистого лантана
Примеры: лантан, церий, прометий, гадолиний, тербий, иттербий, лютеций.
Лантаноиды — это редкоземельные металлы с атомными номерами от 57 до 71. Впервые они были обнаружены в 1787 году в необычном черном минерале (гадолините), обнаруженном в Иттербю, Швеция. Позже минерал был разделен на различные элементы лантаноидов.
Лантаноиды — это металлы с высокой плотностью, плотность которых колеблется от 6,1 до 9,8 г/см³, и они, как правило, имеют очень высокие температуры кипения (1200-3500 °C) и очень высокие температуры плавления (800-1600 °C).
Сплавы лантаноидов используются в металлургии из-за их сильных восстановительных способностей. Около 15 000 тонн лантаноидов ежегодно расходуется в качестве катализаторов и при производстве стекол. Они также широко используются в лазерах и оптических усилителях.
Некоторые исследования показывают, что лантаноиды могут быть использованы в качестве противораковых средств. Лантан и церий, в частности, могут подавлять пролиферацию раковых клеток и способствовать цитотоксичности.
1. Актиниды

Металлический уран, высокообогащенный ураном-235
Примеры: актиний, уран, торий, плутоний, фермий, нобелий, лоренций
Подобно лантаноидам, актиниды образуют семейство редкоземельных элементов с аналогичными свойствами. Они представляют собой серию из 15 последовательных химических элементов в периодической системе от атомных номеров 89 до 103.
Все они радиоактивны по своей природе. Синтетически произведенный плутоний, а также природные уран и торий являются наиболее распространенными актинидами на Земле. Первым актинидом, который был открыт в 1789 году, был уран. И большая часть существующих продуктов актинидов была произведена в 20 веке.
Их свойства, такие как излучение радиоактивности, пирофорность, токсичность и ядерная критичность, делают их опасными для обращения. Сегодня значительная часть (кратковременных) актинидов производится ускорителями частиц в исследовательских целях.
Некоторые актиниды нашли применение в повседневной жизни, например, газовые баллоны (торий) и детекторы дыма (америций), большинство из них используются в качестве топлива в ядерных реакторах и для изготовления ядерного оружия. Уран-235 является наиболее важным изотопом для применения в ядерной энергетике, который широко используется в тепловых реакторах.
Источник https://fb.ru/article/194049/vzaimodeystvie-kislot-s-metallami-vzaimodeystvie-sernoy-kislotyi-s-metallami
Источник https://dedpodaril.com/zoloto/imform/chto-reagiruet-na-zoloto.html
Источник https://new-science.ru/14-razlichnyh-tipov-metallov/

